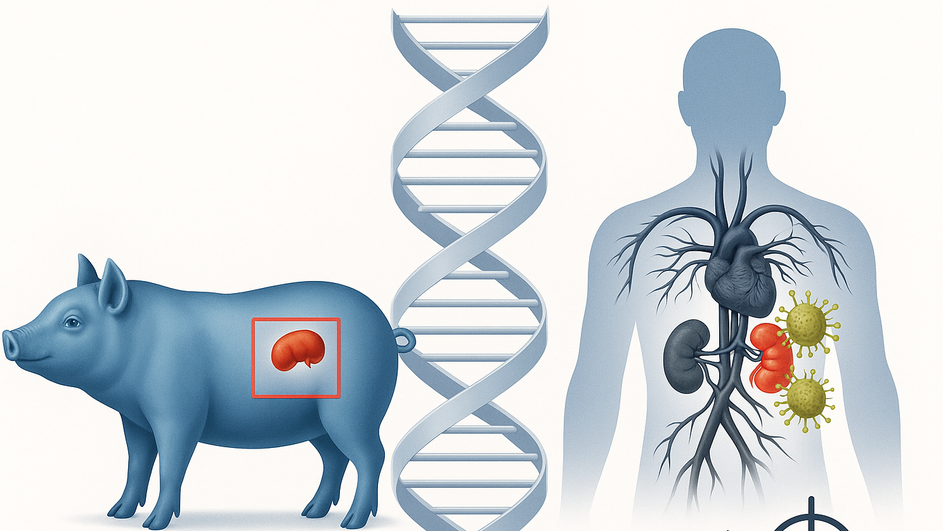
Международная команда ученых из Франции и США под руководством Валентина Гутадье (Paris Institute for Transplantation and Organ Regeneration и NYU Langone) с помощью пространственной транскриптомики отследила, как иммунные клетки проникают в трансплантированную почку свиньи и взаимодействуют с ее тканями. Это позволило точно определить, какие клетки участвуют в отторжении и в какие сроки оно начинается.
Уже на 10-й день после трансплантации в почке появились признаки реакции, связанной с антителами. Максимальная активность иммунитета пришлась на 33-й день, а всего наблюдение продолжалось 61 день. Оказалось, что иммунные клетки (макрофаги и миелоидные) проникали во все ключевые отделы почки. Это подтверждает, что именно они играют главную роль в отторжении. Сообщает ScienceDaily со ссылкой на пресс-релиз конгресса Европейского общества трансплантации органов.
Выявляя конкретное поведение иммунных клеток и экспрессию генов, мы можем усовершенствовать методы лечения отторжения и повысить жизнеспособность трансплантата.
Особенность исследования — в точности. Ученые использовали вычислительную модель, которая позволила отличить человеческие клетки от клеток свиного органа. Это дало возможность построить пространственные карты — где и какие клетки находились, какие гены в них активировались и как менялся характер реакции со временем.
Авторы работы протестировали подходы, которые могли бы замедлить реакцию отторжения. Целенаправленные иммуномодулирующие вмешательства — в том числе терапия, подавляющая ключевые иммунные пути — помогли ослабить молекулярные признаки воспаления. Это подтверждает, что на ранних стадиях отторжения возможно точечное вмешательство, которое позволит сохранить пересаженную почку.
Это исследование закладывает основу для более безопасных и эффективных трансплантаций от свиньи к человеку в ближайшем будущем.
Эти данные особенно актуальны сейчас: в США в 2025 году стартуют первые клинические испытания пересадки почек свиньи живым людям. Новая карта иммунного ответа поможет не только скорректировать генетические изменения у доноров, но и разработать схемы раннего мониторинга и терапии.
Ранее мы сообщали, как исследователи раскрыли клеточные механизмы старения яичников.
