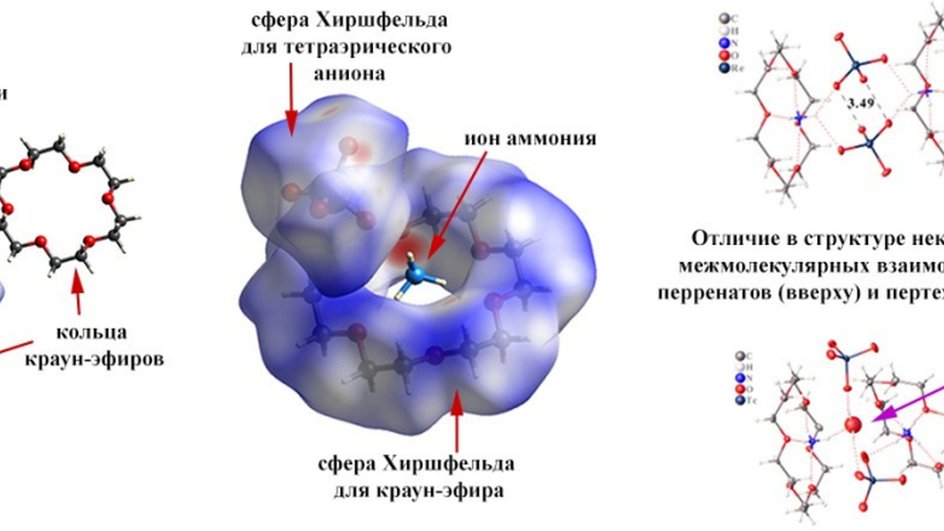
Ученые Института физической химии и электрохимии имени Фрумкина Российской академии наук с коллегами из Кольского научного центра РАН и других российских вузов впервые провели соединение восьми комплексных солей аммония с тетраэдрическим моноанионом с краун-эфирами, выступавшими в роли лигандов (комплексообразователей). По завершению синтеза была исследована кристаллическая структура металлоорганических соединений.
Роль центральных атомов в комплексе играли технеций, рений, осмий и хром. Полученные кристаллы представляли собой моноклинную сингонию. Металлы в соединениях проявляли максимальную степень окисления: Re и Tc — +7, Cr +6 и Os +8.
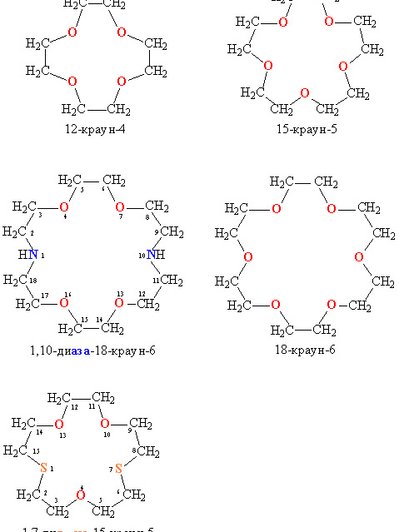
Краун-эфиры были открыты в конце 60-х годов прошлого века. Название соединения получили из-за формы их молекулы, напоминающие многоугольную корону. Эти соединения широко используются в экстракции и разделении малых концентраций химических элементов, супрамолекулярном органическом синтезе, и других, не менее перспективных областях. Однако до сих не было уделено достаточно внимания взаимодействию краун-эфиров с тетраэдрическими комплексами аммония и переходных металлов. Авторы исследования решили восполнить этот пробел.
Тетраэдрический моноанион представляет собой условную равностороннюю треугольную пирамиду. В центре пирамиды расположен атом металла, а в вершинах — атомы кислорода. Иногда один из атомов кислорода может быть замещен галогеном или другими элементами. В экспериментах ученые изучили анионы TcO4, ReO4, CrO3F, OsO3N, CrO3Cl, CrO3Br, а также анионы с неметаллическими центром — BF4 и ClO4.
В присутствии краун-эфиров произошел рост размеров кристаллов и включение водородных связей в систему нековалентных взаимодействий. Аммоний внедрялся внутрь кольца эфира. Все водородные связи образовывались на вершинах пирамиды.
Анализируя синтезированные вещества методом сфер Хиршфельда, ученые обнаружили, что именно физический размер тетраэдрического аниона определяет характер межмолекулярных нековалентных взаимодействий в кристаллах. Между двумя пертехнетат-ионами оказалась встроенной молекула H2O, образовав водородные связи. В перренатах преобладали анион-анионных взаимодействия: тетраэдры «предпочитали» взаимодействовать друг с другом, игнорируя краун-эфиры.
Антон Новиков, научный сотрудник лаборатории радиоактивных материалов ИФХЭ РАН:
Рений принято считать стабильным аналогом радиоактивного технеция, из-за чего у химиков возникла тенденция проводить эксперименты с рением и затем автоматически переносить их результаты на технеций. Наша работа в очередной раз показала, что соединения рения и технеция могут очень сильно отличаться.
В процессе экспериментов перед учеными возникали все новые вопросы. Так, с учетом решающей роли размера аниона при формировании нековалентных межмолекулярных взаимодействий, было решено проверить, как будет вести себя кристаллическая структура вещества, если в вершинах тетраэдров заменить атомы кислорода на атомы серы.
В ходе опытов по термической деструкции соединений было установлено, что наименее стабильными являются соединения осмия, а наиболее «живучими» — соединения рения.
Добыча технеция
Важнейшее прикладное значение экспериментов выразилось в доказательстве того, что присутствие краун-эфиров увеличивает растворимость пертехнетат-иона в смеси воды и хлороформа. Добавление эфира позволило экстрагировать из воды в 30 раз больше технеция, чем экстрагировалось без эфира. Аналогичная картина наблюдалась для осмия и рения. Открытие позволит увеличить эффективность экстракции металлов, роль которых в современных высокотехнологических процессах трудно переоценить.
Технеций (Tc) — самый легкий элемент периодической системы, не имеющий стабильных изотопов. В естественном состоянии в земной коре содержится не более 18 000 тонн технеция-99. Он является продуктом деления тория и урана. Все остальные изотопы созданы искусственно после начала атомной эры.
Период полураспада природного Tc99 составляет 21 тысячу лет. Из синтезированных изотопов долго живут лишь Tc97 и Tc98 — их полураспад длится 420 тысяч лет. Все остальные изотопы проходят полураспад за минуты или часы, в лучшем случае за 90 суток.
Основная сфера применения технеция — ядерная медицина. Также он входит в состав антикоррозионных добавок для оборудования объектов атомной энергетики.

Ранее мы рассказали, что российские ученые получили уникальный коллоидный раствор.
