Метод основан на системе SORT — «селективного нацеливания органов». Ученые модифицировали липидные наночастицы так, чтобы они одновременно проникали в два типа тканей: клетки печени и легкие. Это важно, потому что многие редкие генетические болезни, такие как дефицит альфа-1-антитрипсина (AATD), поражают несколько органов сразу. Результаты опубликованы в журнале Nature Biotechnology.
В AATD поврежденный ген вызывает накопление токсичного белка в печени, а его отсутствие в легких провоцирует эмфизему. До сих пор не существовало способа исправить мутацию одновременно в обеих системах.
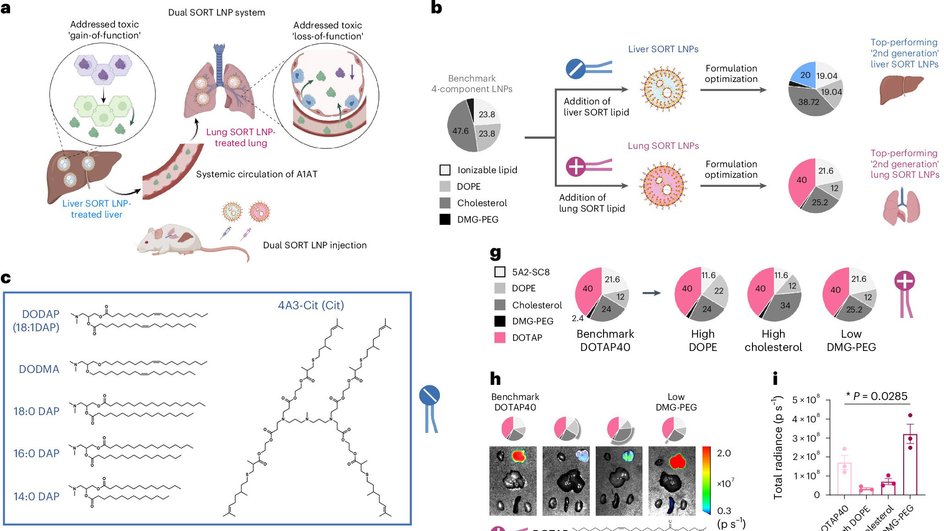
Модифицированные наночастицы редактировали около 40% клеток печени и 10% ключевых клеток легких. Уже через месяц токсичные белки в печени почти исчезли, а в легких активность вредного фермента снизилась на 89%. Эффект в печени сохранялся не менее 32 недель. В клетках, полученных от пациентов, мутация в гене SERPINA1 также была успешно исправлена.
Наши результаты показывают, что SORT может применяться для лечения болезней, затрагивающих сразу несколько органов. В печени уровень мутантного белка снизился на 80%, а активность разрушающего фермента в легких удалось подавить на 89%.
Это первый случай успешного редактирования одного и того же гена в двух органах одновременно. По словам автора исследования Дэниела Зигварта, теперь эту технологию можно адаптировать для других мультисистемных заболеваний.
Ранее мы рассказывали про белок, ответственный за распространение болезни Паркинсона.
